

Perfil de seguridad
de Kanuma®
Para acceder a la Ficha Técnica de Kanuma®, haz click aquí.
PRESENTACIÓN Y PRECIO: KANUMA 2 MG/ML concentrado para solución para perfusión, 1 vial. C.N: 709943. PVL notificado: 8.980 €. Financiado por el Sistema Nacional de Salud.
RÉGIMEN DE PRESCRIPCIÓN Y DISPENSACIÓN: Medicamento sujeto a prescripción médica. Uso Hospitalario. Consulte la Ficha Técnica completa antes de prescribir este medicamento.
Este medicamento está sujeto a seguimiento adicional, es prioritaria la notificación de sospechas de reacciones adversas asociadas a este medicamento.
LAL: lipasa ácida lisosomal; LAL-D: deficiencia de lipasa ácida lisosomal.
Acontecimientos adversos (AA) en lactantes

Desliza la imagen hacia la izquierda para ver más contenido
Acontecimientos adversos (AA) en niños y adultos
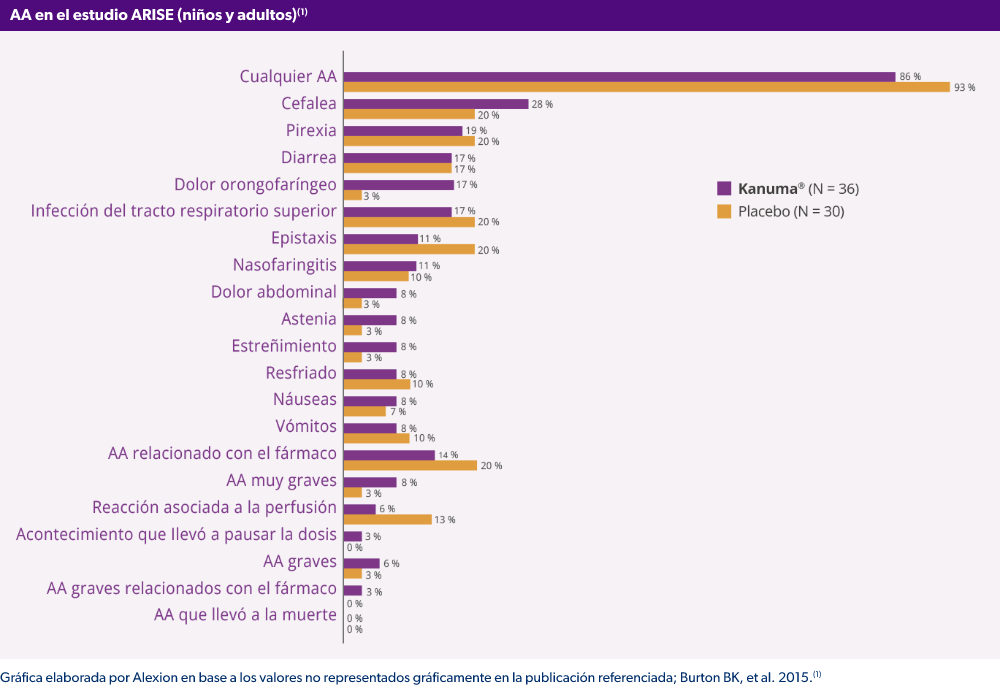
Desliza la imagen hacia la izquierda para ver más contenido

Se recuerda la importancia de notificar las sospechas de reacciones adversas al Centro Autonómico de Farmacovigilancia correspondiente a través del formulario electrónico disponible en https://www.notificaRAM.es
Adicionalmente, se pueden notificar al Departamento de Farmacovigilancia de Alexion en el siguiente contacto: Alexion Pharma Spain S.L. Av. Diagonal, 615, 6ª Planta, 08028 Barcelona (España) Link de notificación de reacciones adversas: https://contactazmedical.astrazeneca.com
Referencias:
- Ficha Técnica Kanuma®. Alexion Europe SAS. Versión Junio 2023.
- Burton BK, Feillet F, Furuya KN, et al. Sebelipase alfa in children and adults with lysosomal acid lipase deficiency: Final results of the ARISE study. J Hepatol. 2022;76(3):577-587.


